Rückblick Biobanken Symposium 2020: Biobanken sind Wegbereiter der COVID-19-Forschung

Das Biobanken-Symposium 2020 - vom 8. bis 10. Dezember. © TMF e.V.
Insgesamt 350 Biobank-Expertinnen und Experten aus ganz Deutschland nahmen vom 8.-10. Dezember 2020 am digitalen 9. Nationalen Biobanken-Symposium 2020 teil. Programmschwerpunkt war das Biobanking während der aktuellen Covid-19-Pandemie in Deutschland. Organisiert wurde das dreitägige Symposium von der Technologie- und Methodenplattform für die vernetzte medizinische Forschung (TMF e. V.) und dem German Biobank Node (GBN).
© TMF e.V.
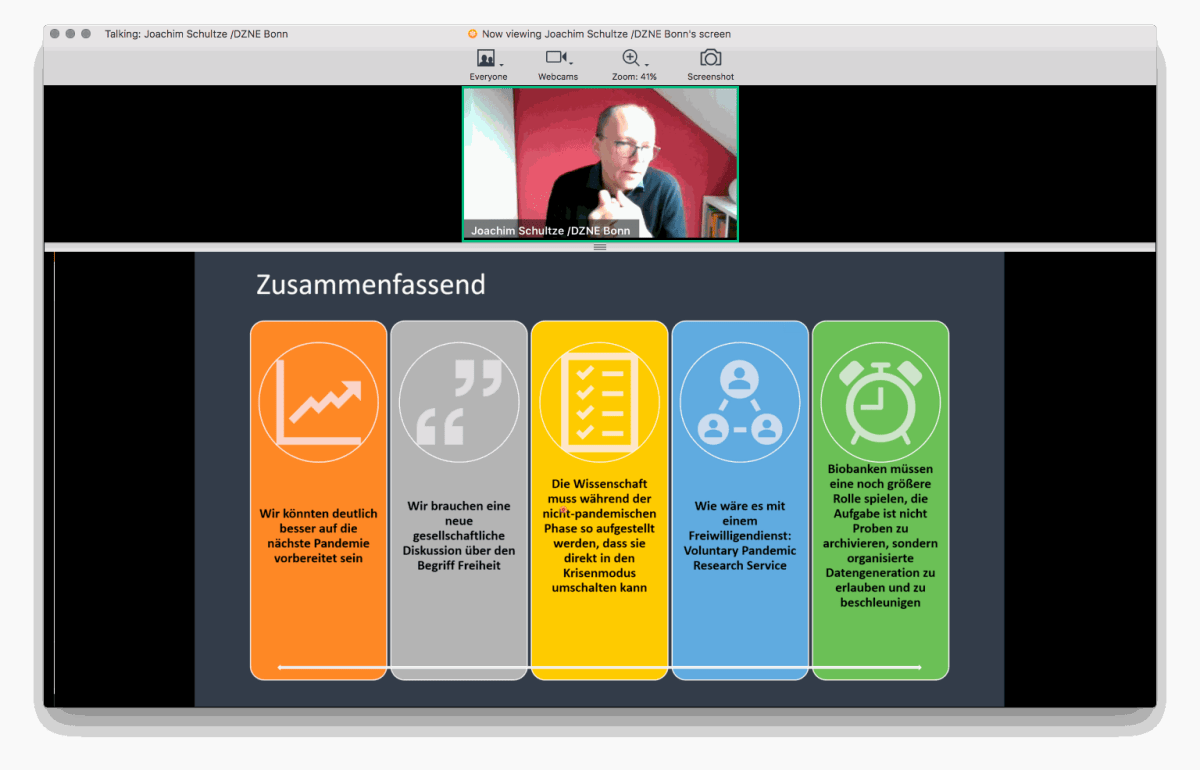
Das Biobanking im Jahr 2020 war geprägt von der Covid-19-Pandemie. Keynote Referent Prof. Dr. Joachim Schultze, Koordinator der Deutschen Covid-19 Omics-Initiative (DeCOI), stellte in seinem Vortrag deshalb die Frage, ob wir auf die Pandemien des 21. Jahrhunderts ausreichend vorbereitet seien. Die Covid-19-Pandemie habe gezeigt, dass die Wissenschaft Kompetenzen bündeln und Synergien herstellen muss, um schnell handlungsfähig zu sein. Prof. Schultze, plädierte deshalb in seiner Keynote dafür, dass „angesichts der Pandemie ein Wandel im System der Wissenschaft notwendig ist. Forscher müssen in diesen Zeiten ohne Einschränkungen zusammenarbeiten und ihre Ergebnisse teilen können, um möglichst schnell zu Erkenntnissen zu gelangen und um auf zukünftige Pandemien besser vorbereitet zu sein.“ Die Aufgabe der Biobanken bestehe nicht primär darin, „Proben zu archivieren, sondern organisierte Datengeneration zu erlauben und zu beschleunigen“, so Schultze.
Biobanking im Kontext Netzwerk Universitätsmedizin (NUM) und Nationales Pandemie Netzwerk (NAPKON)
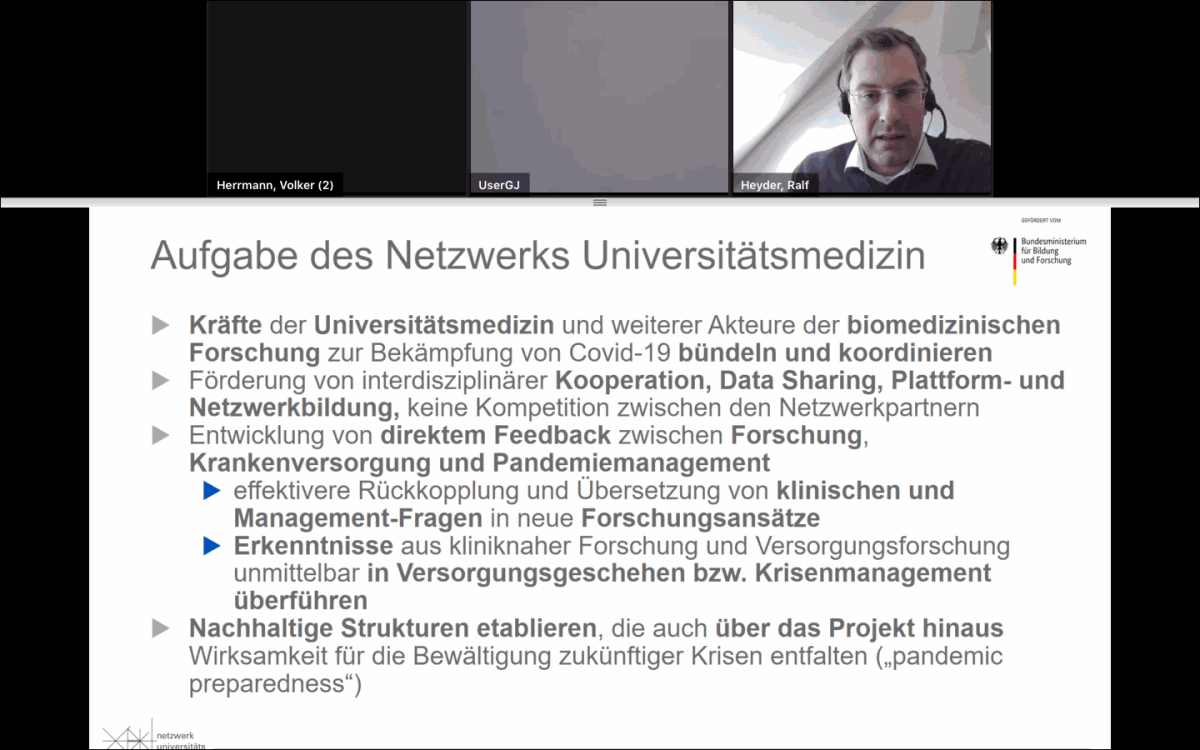
Die aktuellen Entwicklungen im Netzwerk Universitätsmedizin (NUM) stellt der Leiter des NUM, Dr. Ralf Heyder, in seinem Vortrag am 8. Dezember 2020 vor. Das Netzwerk Universitätsmedizin bündelt die Kräfte der Universitätsmedizin und weiterer Akteure der biomedizinischen Forschung in der COVID-19 Forschung. Innerhalb von sechs Monaten wurde mithilfe der Förderung vom Bundesministerium für Bildung und Forschung (BMBF) eine Plattform geschaffen, auf der alle 36 deutschen Universitätskliniken ihre Forschungsaktivitäten zu COVID-19 abstimmen und gemeinsam Daten sammeln und nutzen. Leistungsfähige Infrastrukturen seien die Voraussetzung, um kurzfristige kollaborative Forschungsprojekte wie das NUM aufzusetzen. Ziel sei es, nachhaltige Strukturen zu etablieren, die auch über das Projekt hinaus für die Bewältigung zukünftiger Krisen einsetzbar sind.
Im Rahmen des NUM werden 13 Projekte gefördert, eines davon ist die Kohortenplattform NAPKON. NAPKON baut anhand von COVID-19 ein Netzwerk aus Infrastrukturen mit dem Ziel auf, einen hochqualitativen, repräsentativen COVID-19-Datensatz- und eine entsprechende Bioproben-Zusammenstellung zu erheben.
Biobanken sorgen in NAPKON für eine übergreifende, harmonisierte Sammlung und Nutzung von Bioproben und Daten, erläutert Prof. Dr. Jörg Janne Vehreschild von der Uniklinik Köln. Prof. Dr. Peter U. Heuschmann, Universität Würzburg, legte in seinem Beitrag dar, wie die NAPKON Epidemiological Core Unit (ECU) und der Integrationskern aufgebaut sind - beides integrale Bestandteile der Kohortenplattform.
Dr. Gabriele Anton vom Helmholtz Zentrum München wies anschließend darauf hin, dass hochqualitatives Biobanking deshalb so wichtig sei, weil allein 36 Prozent der nicht-reproduzierbaren Ergebnisse in der präklinischen Forschung auf eine mangelhafte Qualität der Bioproben zurückzuführen sind. Eine möglichst schnelle und lokale Verarbeitung der Proben sei essentiell, um dem entgegenzuwirken. NAPKON setzt deshalb auf die lokale Prozessierung unter Einhaltung standardisierter SOP’s.
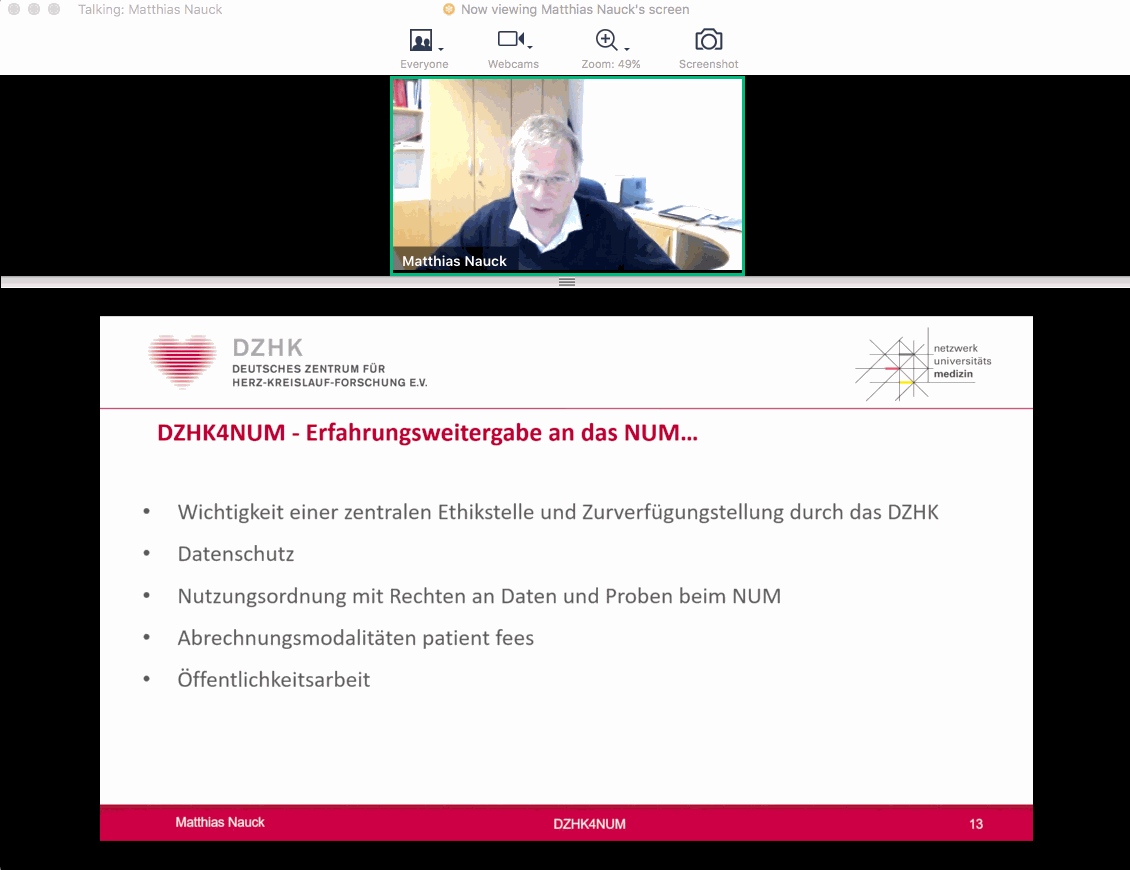
Damit die Daten- und Probenerfassung in NAPKON sofort starten konnte, greift es in der Anfangsphase auf die etablierte Forschungsinfrastruktur des Deutschen Zentrums für Herz-Kreislauf-Forschung (DZHK) zurück. Dafür wurden etablierte Prozesse und Systeme der DZHK-Plattform für Covid-19 erweitert. Prof. Dr. Matthias Nauck von der Universitätsmedizin Greifswald zeigte sich optimistisch, „dass wir einen wichtigen Beitrag zu NUM leisten werden“. Da die Forschungsdateninfrastruktur langfristig angelegt ist, wird diese nach einer Übergangsphase durch die Medizininformatik-Initiative weitergeführt und ausgebaut.
„Die Pandemie zeigt deutlich, welch eng verzahntes und schnell reaktionsfähiges Biobanken-Netzwerk entstanden ist, das der Corona-Forschung exzellente Voraussetzungen bietet,“ kommentierte Prof. Dr. Michael Hummel, Leiter des German Biobank Node (GBN) und der ZeBanC an der Charité Berlin. Hummel berichtet rückblickend aus den vergangenen zehn Monaten, in denen das COVID-19 Biobanking die Biobanken stark gefordert habe. „Ungewöhnliche Situationen erfordern außergewöhnliche Leistungen“, fasst er zusammen. Die Biobanken hätten eine außerordentlich hohe Zahl an Proben verarbeiten müssen, die die jeweiligen COVID-19 Infektionswellen widerspiegelten. Viele Proben haben zu hochrangigen Veröffentlichungen beigetragen.
© TMF e.V.
© TMF e.V.
© TMF e.V.
© TMF e.V.
Validierung von Biobankprozessen: Theorie und Best Practice
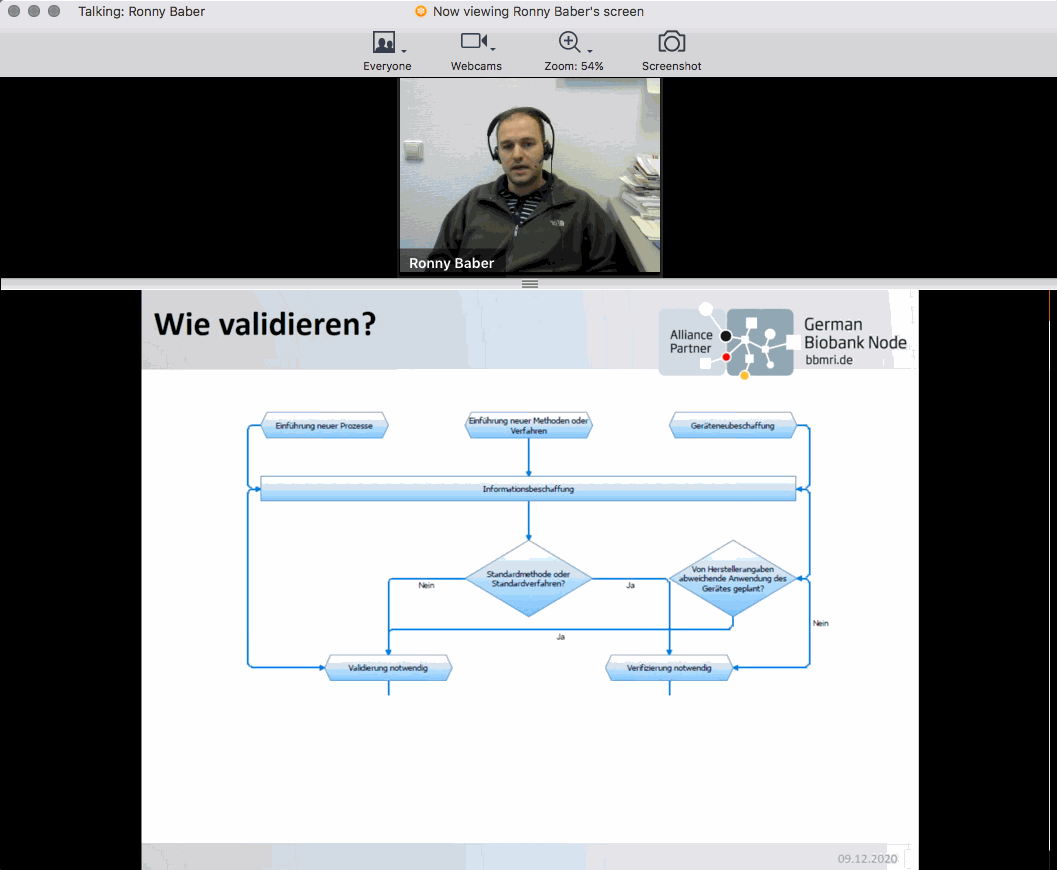
Neu in diesem Jahr war eine Session für technische Mitarbeiterinnen und Mitarbeiter (MTA), welche im Rahmen des Biobanken-Symposiums erstmals stattfand. Zu Beginn der MTA-Session führte Bettina Meinung vom Universitätsklinikum Jena in die Grundlagen der Qualitätssicherung ein und erläuterte, warum man Validierung und Verifizierung in Biobanken braucht.
© TMF e.V.
Dr. Ronny Baber stellte anschließend das Validierungskonzept der Leipzig Medical Biobank vor. Anhand der Validierungs- und Verifizierungskonzepte erläuterte er, was professionelle Biobanken von anderen Sammlungen ohne Qualitätsmanagement unterscheidet. Eine hohe Probenqualität führe zum Vertrauen der Nutzer und sei eine Frage der Nachhaltigkeit der Biobank, erklärte Baber.
Dr. Heidi Altmann, Technische Universität Dresden, sprach anschließend über die „Validierung eines vollautomatisierten Robotik-Systems für die Isolation von mononukleären Zellen aus Blut und Knochenmark für das Biobanking“. Die Biobank Dresden ist auf zelluläres Biobanking, insbesondere von sogenannten mononuklearen Zellen aus Blut und Knochenmark, spezialisiert.
Dr. Michael Neumann, Universitätsklinikum Würzburg, sprach abschließend in seinem Vortrag über Software Validierung. Die Validierung prüft, ob einer Software die Bedürfnisse der Nutzer in einem typischen Nutzungskontext erfüllt. “Verifizierung entdeckt keine Fehler in der Spezifikation, deshalb brauchen wir Validierung”, erläutert Neumann.
Ethik und Datenschutz
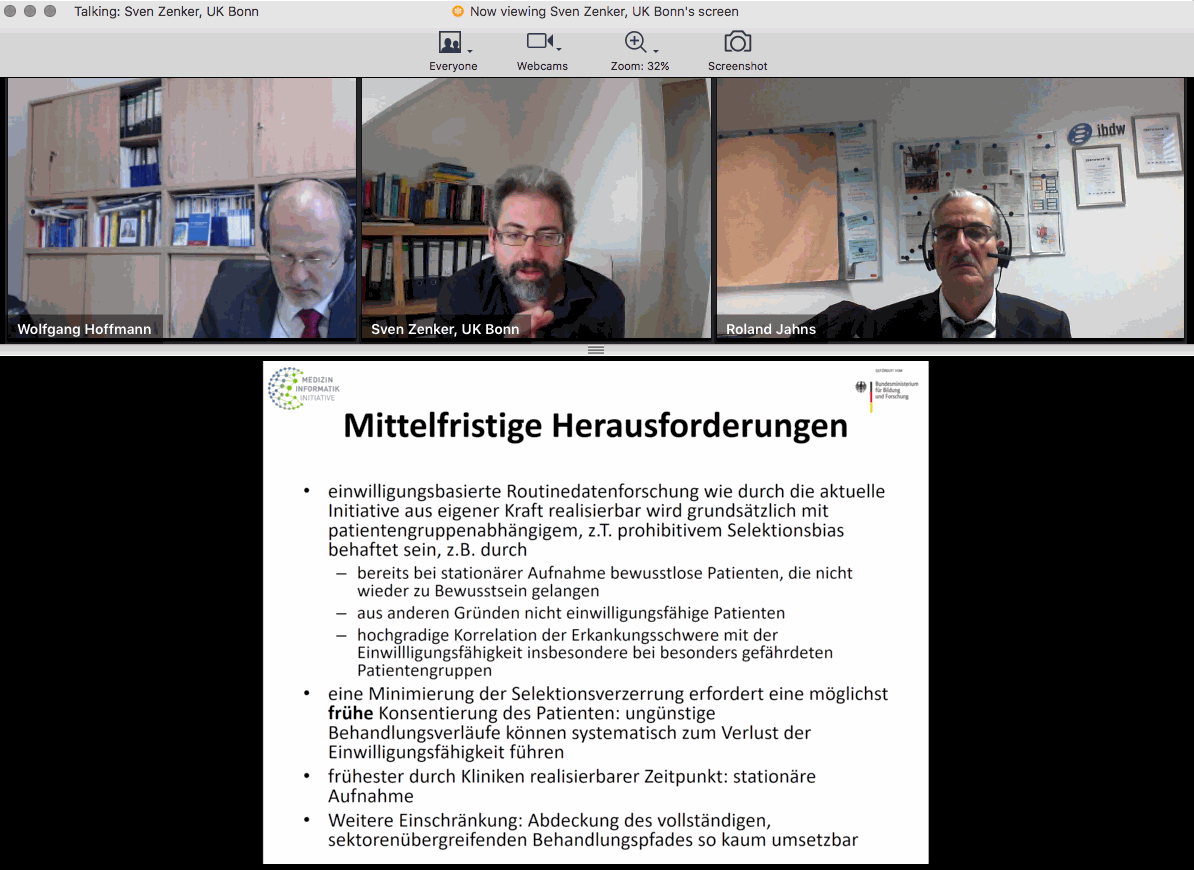
In der Session „Ethik und Datenschutz“ gab PD Dr. Sven Zenker vom Universitätsklinikum Bonn einen Einblick in den aktuellen Stand der breiten Einwilligung ("Broad Consent") in der Medizininformatik-Initiative (MII).
Der Broad Consent ist die rechtliche Grundlage zur Datennutzung im Rahmen der MII. Alle Datenschutzaufsichtsbehörden der Länder und des Bundes haben diesen im April 2020 akzeptiert. Damit können Patienten erstmalig auf Basis der EU-Datenschutzgrundverordnung bundesweit einheitlich eine Einwilligung in die Nutzung ihrer pseudonymisierten klinischen Daten geben. Die medizinische Forschung kann diese für vielfältige, nicht auf eine Erkrankung beschränkte Forschungszwecke verwenden. Dies ist ein Meilenstein für die Initiative und die medizinische Forschungslandschaft in Deutschland.
Die Sicht der Ethikkommissionen auf den Broad Consent erläuterte Prof. Dr. Georg Schmidt, Vorstandsmitglied im AK EK: Patientinnen und Patienten müssten selbstbestimmt entscheiden, ob sie an einer Studie teilnehmen möchten. Weiterhin müssen die betroffenen Patientinnen und Patienten entscheidungsfähig und ausreichend informiert sein sowie in die Lage versetzt werden, Nutzen und Risiken hinreichend abzuwägen. Ethikkommissionen votieren meist in einem zweistufigen Verfahren zur Breiten Einwilligung: zuerst geben sie ein Votum zum Konzept der Biobank, danach votieren sie die einzelnen Projekte bezüglich ihrer Sinnhaftigkeit und der ergriffenen Maßnahmen zum Datenschutz. Die Mustertexte des AK EK und der MII erlauben eine adäquate Aufklärung zu Sinn und Risiken der Breiten Einwilligung, so Schmidt.
Anschließend berichtet Prof. Dr. Wolfgang Hoffmann vom Universität Greifswald über die Implementation des "Broad Consent" am Uniklinikum Greifswald und dessen empirische Begleitung. Die Forschungsfrage zielte darauf ab, wie prä- und teilstationär aufgenommene Patientinnen und Patienten die zwei möglichen Varianten des geplanten Aufklärungsgespräches zur wissenschaftlichen Nutzung ihrer Routinedaten wahrnehmen und welche Bedürfnisse sie im Hinblick auf die Ausgestaltung zentraler Prozessdetails artikulieren. Die Studienteilnehmer und -teilnehmerinnen zeigten eine hohe Zufriedenheit mit beiden Prozessvarianten. Die Aufklärung direkt nach dem Aufnahmegespräch in der Patientenaufnahme sei am effektivsten, so Hoffmann.
Einen Ausblick in die Zukunft gibt Prof. Dr. Michael Krawczak vom Universitätsklinikum Schleswig-Holstein in seinem Vortrag „Beyond traditional informed consent: Neue Überlegungen und Konzepte zur Datenspende“. In seiner Stellungnahme „Big Data und Gesundheit“ hat der Deutsche Ethikrat 2017 das Konzept einer „Datenspende“ für die medizinische Forschung eingeführt. Im Auftrag des Bundesgesundheitsministeriums hat die TMF gemeinsam mit einer interdisziplinären Gutachtergruppe unterschiedliche Modelle einer möglichen Datenspende für die medizinische Forschung skizziert und bewertet. Das Gutachten, welches Modelle der „Datenspende“ definiert, ethisch bewertet sowie unterschiedliche konkrete Ausgestaltungsoptionen der „Datenspende“ in Deutschland vorschlägt, ist im Sommer 2020 erschienen. Die Gutachter fordern unter anderem, die zeitliche und räumliche Entkopplung der Einwilligung der Datenspender vom Kontext einer medizinischen Behandlung. Weiterhin sollte die informierte Einwilligung der Datenspender durch ein einfach auszuübendes Widerspruchsrecht ersetzt werden (Opt-out). Dafür müsste jedoch eine bundeseinheitliche gesetzliche Regelung zum Forschungsdatenschutz und infrastrukturelle Voraussetzungen für eine Datenspende geschaffen werden.
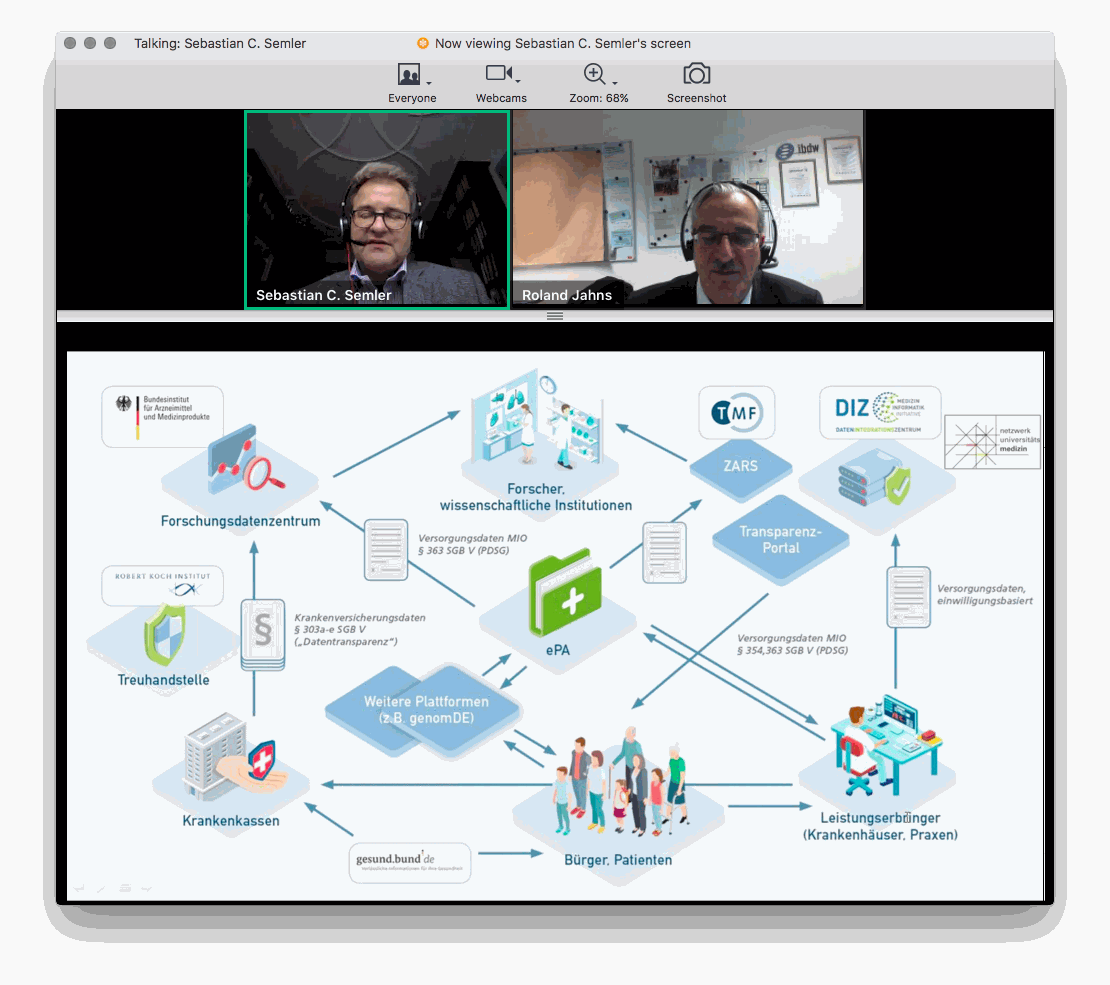
Sebastian C. Semler, Geschäftsführer der TMF e. V., gab schließlich in seinem Vortrag einen Ausblick, was die forschungskompatible EPA konkret für die Forschung bedeuten wird. Ab 1.1.2023 wird diese nach derzeitiger Zeitplanung zur Verfügung stehen und eine Datenspende für die Forschungsnutzung ermöglichen. Die ePA-Inhalte werden strukturiert und anhand internationaler Standards spezifiziert. Bis dahin sei noch die Antragsgovernance zu klären und ein übergreifendes ID- und Consent-Management aufzusetzen. Ebenso müssen ein Pseudonymisierungsdienst bereitgestellt und die Schnittstellen zwischen Leistungserbringern, Patienten und Forschenden definiert werden, so Semler.
© TMF e.V.
© TMF e.V.
© TMF e.V.

© TMF e.V.
IT und Qualitätsmanagement
Der dritte und letzte Tag des Biobanken Symposiums 2021 widmete sich dem Schwerpunktthema „IT und Qualitätssicherung“. Andrea Wutte vom europäischen Biobanken-Netzwerk BBMRI-ERIC sprach darüber, wie Biobanken und klinische Studien noch besser zusammenarbeiten können. Frau Wutte lobte das hohe Niveau, auf dem deutsche Biobanken im europäischen Vergleich arbeiten. BBMRI-ERIC als europäischer Dachverband setze sich dafür ein, die Standardisierung von Biobanken mithilfe der Weiterentwicklung von ISO-Standards voranzubringen. Prof. Dr. Petr Holub, BBMRI-ERIC, erläuterte anschließend die BBMRI-ERIC Services for Discovering and Accessing Biobanks.
© TMF e.V.
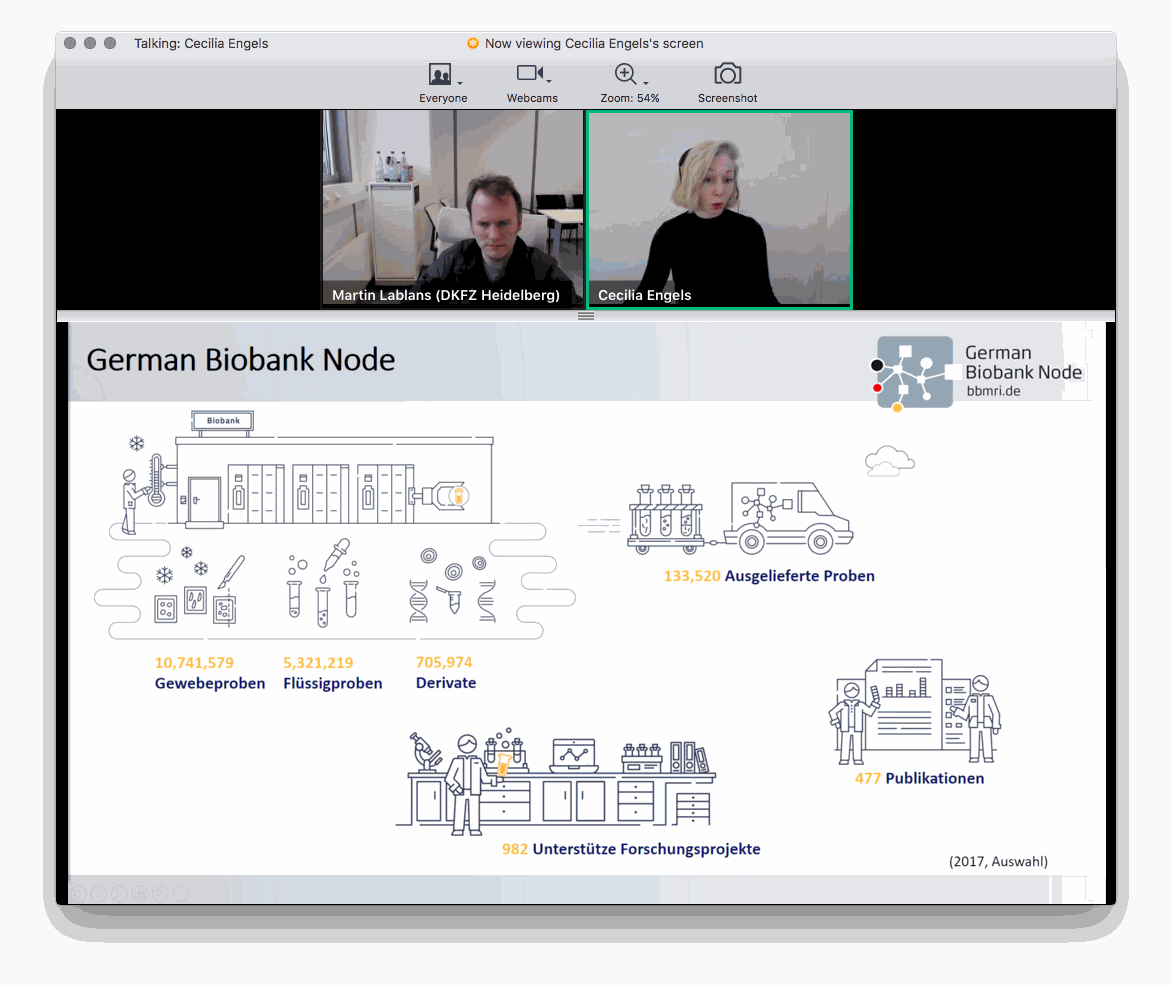
Dr. Cecilia Engels, (GBN), Dr. Björn Kroll, Universität zu Lübeck, und Alexander Kiel, Universität Leipzig, präsentierten in Ihren Vorträgen die IT-Infrastruktur der German Biobank Alliance (GBA), von der der sogenannte Sample Locator ein zentraler Bestandteil ist. Fr. Engels stellte dar, dass im Jahr 2017 von 16 Millionen in Biobanken gelagerten Proben nur 130.000 für die Forschung genutzt wurden. Aufgabe des Sample Locator sei es, Wissenschaftlerinnen und Wissenschaftlern die zentrale Bioprobensuche in den 42 an das Netzwerk angeschlossenen akademischen Biobanken zu ermöglichen. Das Online-Suchtool wurde von einem interdisziplinären Entwicklerteam der GBA unter dem Dach des GBN entwickelt. Zwischen Mai und Juli 2020 wurden 896 Suchanfragen gestellt. „Es gibt noch Luft nach oben. Wir wollen noch mehr Proben in wissenschaftliche Projekte liefern“, resümiert Engels.
© TMF e.V.
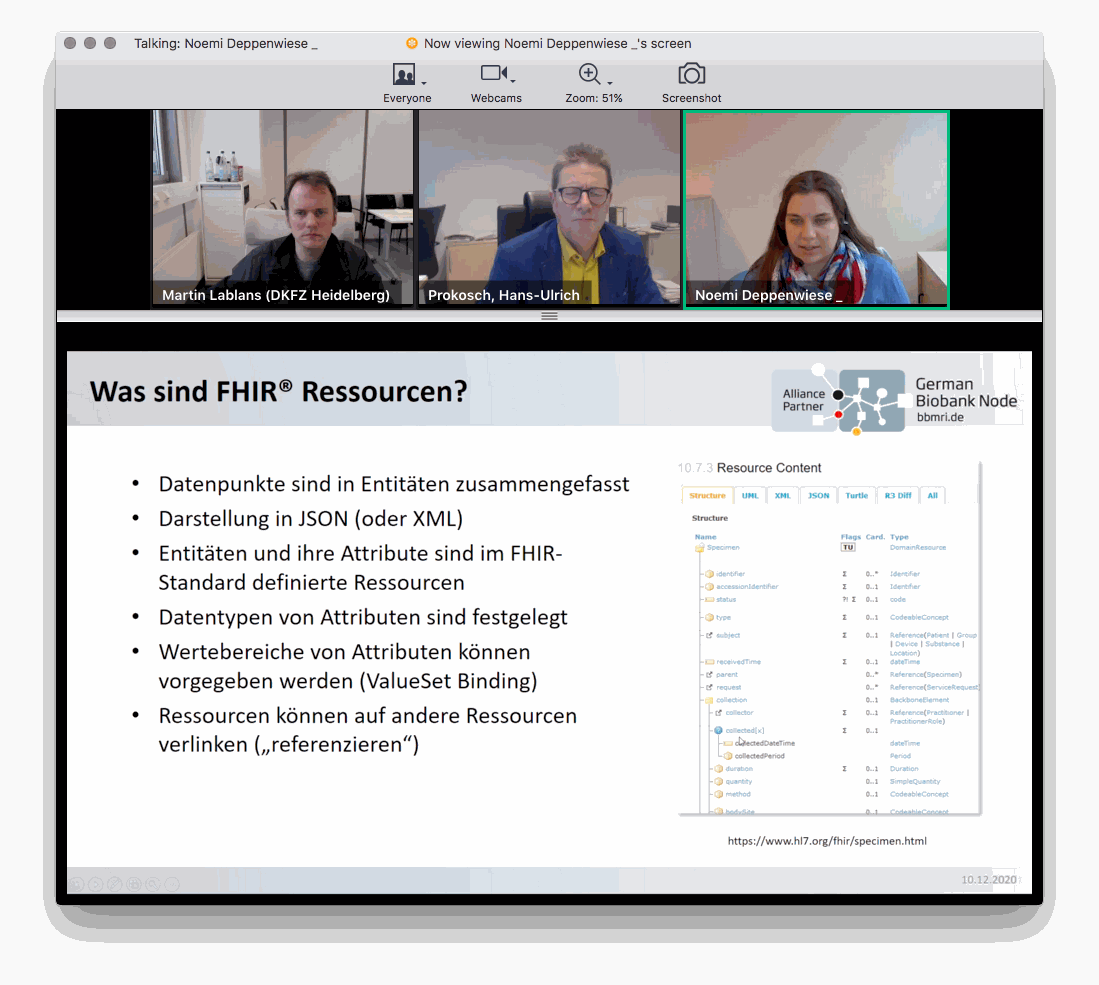
Wie Bioproben und Daten zukünftig noch enger zusammenrücken, erläutern Noemi Deppenwiese, und Prof. Dr. Hans-Ulrich Prokosch, beide von der Friedrich-Alexander-Universität Erlangen-Nürnberg sowie Prof. Dr. Michael Hummel (GBN). Der Kerndatensatz der Medizininformatik-Initiative (MII) wurde um ein Erweiterungsmodul Biobanken ergänzt, welcher nach einer Kommentierungsphase im Rahmen des ab Mai 2021 startenden Projekts ABIDE_MI implementiert werden soll. Damit in Zukunft die Biobanken und Daten enger vernetzt werden können, ist die Verbindung der Biobanken mit der Medizininformatik-Initiative in Form des Projektes ABIDE geplant, erläutert Prof. Prokosch in seinem Vortrag. Möglich wird das mithilfe eines zentralen FHIR-basierten, MII-weiten Abfrage- und Analyseportals, welches in die Zentrale Antrag- und Registerstelle (ZARS) der MII eingebunden ist. So können zukünftig standardisiert Patientendaten mit Informationen über assoziierte Bioproben verknüpft, und Bioproben, die im Kontext der Patientenversorgung erhoben werden, von Unikliniken gesammelt werden.
Sebastian C. Semler, Geschäftsführer der TMF, erläutert:
ABIDE_MI wird einen interdisziplinären Ansatz verfolgen, der die Errungenschaften und Erfahrungen der MII und der Biobanken der GBA in einer nachhaltigen Gesundheits-IT-Infrastruktur zusammenführt.
Über die Veranstaltung
Das Nationale Biobanken Symposium ist der größte jährliche Branchentreff der akademischen Biobanken-Community in Deutschland. Im Mittelpunkt stehen der Informations- und Wissensaustausch zu organisatorischen, ethischen und infrastrukturellen Entwicklungen im Biobanking. Im Jahr 2020 fand das Biobanken Symposium aufgrund des Pandemiegeschehens erstmals digital statt und erfreute sich einer großen Reichweite. Alle Sessions waren ausgebucht. Das 10. Nationale Biobanken Symposium 2021 soll nachderzeitigem Planungsstand im Dezember 2021 wieder in Präsenz in Berlin stattfinden. Ein Termin wird rechtzeitig bekannt gegeben.
Weiterführende Informationen


